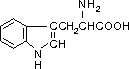АМИНОКИСЛОТЫ, органические (карбоновые) кислоты, содержащие, как правило, одну или две аминогруппы (-NH2).В зависимости от положения аминогруппы в углеродной цепи по отношению к карбоксилу различают α-, β-, γ- и т. д. аминокислоты. В природе широко распространены α-аминокислоты, имеющие (кроме глицина) один или два асимметрических атома углерода и, в основном, L-конфигурацию. В построении молекул белка участвуют обычно около 20 L-α-аминокислот (пролин — α-аминокислота). Специфическая последовательность чередования аминокислот в пептидных цепях, определяемая генетическим кодом, обусловливает первичную структуру белка. Высшие растения и хемосинтезирующие организмы все необходимые им аминокислоты синтезируют из аммонийных солей и нитратов (в растительной клетке они восстанавливаются до NH3) и кето- или оксикислот — продуктов дыхания и фотосинтеза. Человек и животные синтезируют большинство так называемых заменимых аминокислот из обычных безазотистых продуктов обмена и аммонийного азота; незаменимые аминокислоты должны поступать с пищей. Занимают центральное место в обмене азотистых веществ (входят в состав белков, пептидов, участвуют в биосинтезе пуринов, пиримидинов, витаминов, медиаторов, алкалоидов и других соединений). В организме окислительный распад аминокислот путём дезаминирования (особенно интенсивно идёт в почках и печени) главным образом глутаминовой кислоты, образовавшейся путём переаминирования, приводит к образованию кето- и оксикислот — промежуточных продуктов цикла трикарбоновых кислот. Далее они превращаются в углеводы, новые аминокислоты и т. п. или окисляются до СО2 и H2O с выделением энергии. При этом азот в виде аммонийных солей, мочевины и мочевой кислоты выводится из организма. У растений связанный азот используется более полно и азотистые отходы практически отсутствуют. В тканях живых организмов встречаются аминокислоты (свыше 100), не входящие в состав белков. Среди них важные промежуточные продукты обмена веществ (орнитин, цистатионин и другие), а также редкие аминокислоты, биологические функции которых неясны. В микробиологической промышленности используют способность мутантных штаммов некоторых микроорганизмов продуцировать отдельные аминокислоты (глутаминовую кислоту, лизин и другие). Аминокислоты, а также их смеси, применяют в медицине, животноводстве (для обогащения кормов), как и сходные продукты для промышленного синтеза полиамидов, красителей. Многие аминокислоты получены абиогенным путём в условиях, моделирующих атмосферу первобытной Земли.
Общая формула альфа-аминокислот:
![]()
Важнейшие аминокислоты входящие в состав белка
Одноосновные моноаминокислоты
Аланин (Ала, Ala)
![]()
Валин (Вал, Val)
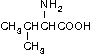
Глицин (Гли, Gly)
![]()
Изолейцин (Иле, Ile)
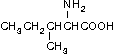
Лейцин (Лей, Leu)
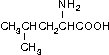
Метионин (Мет, Met)
![]()
Серин (Сер, Ser)
![]()
Тирозин (Тир, Tyr)
![]()
Треонин (Тре, Thr)
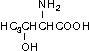
Фенилаланин (Фен, Phe)
![]()
Цистеин (Цис, Cys)
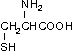
Двухосновные моноаминокислоты
Аспаргиновая кислота (Асп, Asp)
![]()
Глутаминовая кислота (Глу, Glu)
![]()
Одноосновные диаминокислоты
Аргинин (Арг, Arg)
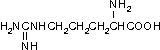
Лизин (Лиз, Lys)
![]()
Аминокислоты,
содержащие амидную группу
Аспарагин (Асн, Asn)
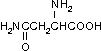
Глутамин (Глн, Gln)
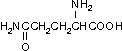
Аминокислоты,
содержащие гетероциклические кольца
Гистидин (Гис, His)
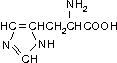
Пролин (Про, Pro)
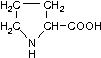
Триптофан (Трп, Trp)